Hsp70
HSP veut dire Heat Shock Protein. Ce sont en fait des protéines chaperonnes, de classe 1. En effet, elles sont guarantes de la bonne conformation des protéines de la cellule, et les aides à se protéger des stress externes,.
HSP veut dire Heat Shock Protein. Ce sont en fait des protéines chaperonnes, de classe 1. En effet, elles sont guarantes de la bonne conformation des protéines de la cellule, et les aides à se protéger des stress externes[1], [2].
Découverte
Les membres de la famille Hsp70 sont fortement régulatrice du stress dû à la chaleur et les produits chimiques toxiques, surtout les métaux lourds comme l'arsenic, le cadmium, cuivre, mercure, etc. Hsp70 a été originellement découverte par Ritossa FM dans les années 1960 lorsque un travailleur de laboratoire a accidentellement augmenté la température d'incubation d'une culture de Drosophilas (mouches des fruits). Lors de l'examen des chromosomes, Ritossa trouvé une augmentation de la transcription des gènes d'une protéine inconnue. [3][4] Cela fut plus tard décrit comme la «Heat Shock Response» et les protéines ont été nommé «Heat Shock Proteins» (Hsps).
Structure
Toutes les protéines Hsp70 ont trois grands domaines fonctionnels.
- Un domaine N-terminal du domaine ATPase lie l'ATP (adénosine triphosphate) et hydrolyse l'ADP (adénosine diphosphate). L'échange de l'ATP réalise des changements conformationnels dans les deux autres domaines.
- Un domaine de fixation du substrat avec une affinité pour les molécules neutres, d'acides aminés hydrophobes résidus. Le domaine est suffisamment long pour interagir avec des peptides jusqu'à sept résidus de longueur.
- Un domaine C-terminal riche en structure en hélice alpha, qui agit comme un «couvercle» pour le domaine de fixation du substrat. Lorsque une protéine Hsp70 est lié à l'ATP, le couvercle est ouvert et relâche assez rapidement le peptide. Quand les protéines Hsp70 sont liés à l'ADP, le couvercle est fermé, et les peptides sont étroitement liés au domaine de fixation du substrat.
Fonction et régulation
La chaleur est un des plus grands ennemis des protéines puisque cela modifie le reploiement et donc, altère la fonction de la protéine. Par conséquent, l'évolution a mis en place des dispositifs permettant d'éviter cette dénaturation par la chaleur pour ne pas avoir à remplacer trop fréquemment les protéines dénaturées (le recyclage des protéines est nommé le «turn-over»). Le rôle des HSP est de garantir la bonne conformation des protéines dans la cellule.
Les HSP se distinguent par le fait qu'elles possèdent plus d'acides aminés capables d'établir de fortes interactions entre eux que les protéines «normales», c'est-à-dire, non-HSP. Donc, les HSP sont par conséquent moins «flexibles» et moins sensibles à la chaleur.
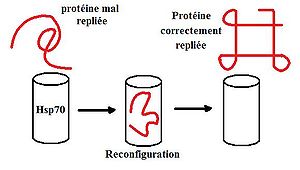
Concrètement, une HSP s'approche d'une protéine. Selon que la conformation de la protéines soit bonne ou mauvaise, elle permettra ou non l'association de la HSP ou sera dirigée vers le protéasome pour être dégradée. Si la HSP s'est associée, cette dernière va servir de «squelette» à la protéine ce qui lui évite de se faire déformer (dénaturer) par la chaleur. Plus tard, les deux protéines se séparent et continuent leur vie dans la cellule.
Le terme «HSP» regroupe en fait toute une famille de protéines, chacune ayant un partenaire protéique spécifique. Certaines HSP sont exprimées (synthétisées) tout le temps tandis que d'autres sont exprimées suite à une brusque augmentation de la température.
Cancer
HSP 70 est surexprimé dans les mélanomes malins et sousexprimé dans les cellules rénales cancéreuses.
Membre de la famille
Les procaryotes expriment trois protéines Hsp70 : DnaK, HscA (Hsc66), et HscC (Hsc62). [5]
Les organismes eucaryotes expriment plusieurs protéines Hsp70 un peu différentes (car particulièrement conservées au cours de l'évolution étant donné qu'elles sont principales). Toutes partagent la même structure de domaine, mais chacune a un modèle unique d'expression.
- Hsc70 (Hsp73/HSPA8) est constitutivement dite protéine chaperon. Elle représente le plus souvent un à trois pour cent du total des protéines cellulaires.
- Hsp72 (HSPA1A) est une protéine induite par le stress. Des concentrations élevés peuvent être produites par les cellules en réponse à une hyperthermie, un stress oxydatif, et des changements de pH.
- Binding immunoglobulin protein (BIP ou Grp78) est une protéine située au niveau du réticulum endoplasmique. Elle est impliqué dans le repliement des protéines, et sa concentration et foncion fluctue en réponse au stress ou à la famine.
- mtHsp70 ou Grp75 est la Hsp70 mitochondriale.
Ce qui suit est une liste des gènes d'Hsp70 de l'homme et de leurs protéines correspondantes :[1]
| gèn" | proteine | synonymes | localisation cellulaire |
|---|---|---|---|
| Hsp70-1a | HSP70-1, Hsp72 | Noyau/Cyto | |
| Hsp70-1b | HSP70-2 | Nuc/Cyto | |
| Hsp70-1L | ? | ||
| Hsp70-2 | ? | ||
| Hsp70-4 | ? | ||
| Hsp70-4L | ? | ||
| Hsp70-5 | BiP/Grp78 | ||
| Hsp70-6 | ? | ||
| Hsp70-7 | ? | ||
| Hsp70-8 | Hsc70 | Nuc/Cyto | |
| Hsp70-9 | Grp75/mtHsp70 | ||
| Hsp70-12a | ? | ||
| Hsp70-14 | ? |
References
- Tavaria M, Gabriele T, Kola I, Anderson RL, «A hitchhiker's guide to the human Hsp70 family», dans Cell Stress Chaperones, vol. 1, no 1, April 1996, p. 23–8 [lien PMID]
- ↑ Morano KA, «New tricks for an old dog : the evolving world of Hsp70», dans Ann. N. Y. Acad. Sci. , vol. 1113, October 2007, p. 1–14 [lien PMID lien DOI]
- ↑ Ritossa F, «A new puffing pattern induced by temperature shock and DNP in drosophila», dans Cellular and Molecular Life Sciences (CMLS) , vol. 18, no 12, 1962, p. 571-573 [lien DOI]
- ↑ Ritossa F, «Discovery of the heat shock response», dans Cell Stress Chaperones, vol. 1, no 2, June 1996, p. 97–8 [lien PMID]
- ↑ Yoshimune K, Yoshimura T, Nakayama T, Nishino T, Esaki N, «Hsc62, Hsc56, and GrpE, the third Hsp70 chaperone system of Escherichia coli», dans Biochem. Biophys. Res. Commun. , vol. 293, no 5, May 2002, p. 1389–95 [lien PMID lien DOI]
Recherche sur Google Images : |
|
"Hsp70 family members contain" L'image ci-contre est extraite du site assaydesigns.com Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (800 x 800 - 122 ko - jpg)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 05/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité