Actine
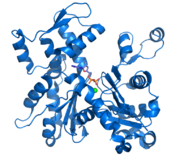
L'actine est une protéine bi-globulaire de 5,46nm de diamètre importante pour l'architecture et les mouvements cellulaires.
| Actine | |
|---|---|
| Caractéristiques générales | |
L'actine est une protéine bi-globulaire de 5, 46nm de diamètre importante pour l'architecture et les mouvements cellulaires. Elle est présente dans l'ensemble des cellules du corps (protéine ubiquitaire), et particulièrement dans les cellules musculaires. Elle peut représenter jusqu'à 10% de la masse totale protéique des cellules. Cette protéine a été hautement conservée lors de l'évolution des eucaryotes, puisque l'identité entre un isotype d'actine humaine et l'actine de levure (S. cerevisiæ) est supérieur à 90%. La majorité des cellules eucaryotes possèdent de nombreux gènes d'actine codant des protéines un peu différentes.
Structure
Chez les mammifères, il existe 7 isotypes d'actine :
- 4 isoformes d'actines alpha (présentes dans les muscles striés squelettiques et cardiaque et les muscles lisses),
- 2 isoformes d'actines gamma (présentes dans le muscle lisse entérique et dans les tissus non musculaires),
- 1 isoforme d'actine beta (non musculaire).
L'actine est une protéine dont le diamètre est de 5, 5 nm, qui contient un acide aminé rare : la 3-méthyl histidine. Elle est constituée par un polypeptide de 375 acides aminés. Dans la cellule, on la retrouve sous deux formes :
- Actine G (Globulaire), forme monomérique soluble en solution aqueuse.
Le monomère d'actine G est associé à un cation divalent tel que l'ion calcium ou le magnésium (le magnésium in vivo) et un nucléotide de type ATP ou ADP selon l'état de phosphorylation du nucléotide. En l'absence de ces deux cofacteurs, l'actine se dénature aisément. La thymosine bloque la polymérisation en s'associant aux monomères d'actine G liée à l'ATP.
- Actine F (Filamenteuse) ou microfilament, de 7 nm de diamètre et qui est un polymère d'actine G.
Ce filament est un arrangement hélicoïdal dextre, avec un tour d'hélice comportant 13 monomères et d'une longueur de 37nm
Polymérisation
Elle débute par une phase dite de nucléation durant laquelle des dimères (ou trimères) d'actine (appelés noyaux) s'assemblent. Cette étape, défavorable thermodynamiquement, est une étape lente. Si la concentration en monomères d'actine (actine dite G) est supérieure à une concentration critique, l'actine G s'assemble en filaments à partir des noyaux préformés. C'est l'étape d'élongation des filaments. Cette étape rapide est fréquemment nommée phase de polymérisation, quoique l'actine filamenteuse (dite actine-F) ne soit pas un véritable polymère (les monomères ne sont pas liés entre eux par une liaison covalente au sein d'un filament). Une fois constitués, les filaments d'actine sont à l'équilibre entre dissociation des filaments aux extrémités et association de monomères aux extrémités. Dans les cellules, la formation spontanée de noyaux d'actine est particulièrement défavorable. Aussi, les cellules ont recours à des protéines dites nucléateurs. À ce jours, trois nucléateurs ont été identifiés : le complexe Arp2/3 (complexe composé de 7 sous unités protéiques), les formines, et la protéine Spire.
Localisation et rôle
Dans la contraction musculaire, l'actine polymérisée se lie à une autre protéine, la myosine. Cette dernière s'accroche au polymère d'actine et la fait coulisser comparé à elle; à l'autre bout du filament d'actine, un autre filament de myosine fait la même chose de façon symétrique; les deux filaments de myosine se rapprochent par conséquent l'un de l'autre, c'est la contraction musculaire.
Autres rôles :
- Anneau contractile des cellules en division lors de la cytodiérèse servant à séparer les cellules issues de la mitose (ou de la méiose).
- Ceinture de desmosomes au pôle apical des cellules épithéliales.
- Maintien des microvillosités des cellules épithéliales intestinales.
- Émission de lamellipodes qui autorisent la cellule de s'allonger dans une direction donnée ce qui permet la migration cellulaire ou la prise de proies (chez les amibes et les cellules phagocytaires du dispositif immunitaire comme les macrophages). Dans le cas de la migration cellulaire, les microfilaments d'actine se lient à des points d'adhésion focaux qui servent de points d'appui sur la matrice extracellulaire, nécessaires pour avancer. Ce sont les protéines associées aux intégrines qui se lient à l'actine.
Voir aussi
Recherche sur Google Images : |
|
"Microfilament d'actine" L'image ci-contre est extraite du site virologie.free.fr Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (466 x 318 - 21 ko - gif)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 05/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité